Obsah
- Hlavný rozdiel
- Porovnávacia tabuľka
- Čo sú to iónové zlúčeniny?
- Čo sú to molekulárne zlúčeniny?
- Iónové zlúčeniny verzus molekulárne zlúčeniny
Hlavný rozdiel
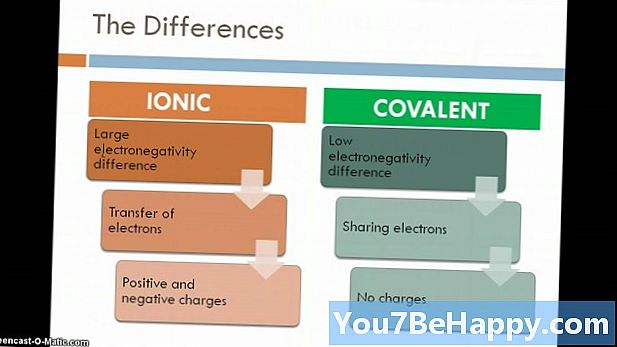
Zlúčenina sa rozpoznáva ako látka, ktorá sa vytvára, keď sa dva alebo viac prvkov spoja v určitých pomeroch chemickou väzbou. Iónová zlúčenina je zlúčenina vytvorená v dôsledku elektrostatickej sily príťažlivosti medzi kovmi a nekovmi. Obvykle sa iónové zlúčeniny objavujú v predanom kryštalickom stave. Ďalej sú iónové zlúčeniny dobrými vodičmi elektriny a majú vysoké teploty topenia a teploty varu. Na druhej strane sú molekulárne zlúčeniny tvorené v dôsledku zdieľania elektrónov medzi dvoma nekovmi. Vo vzťahu k iónovej zlúčenine sú zlým vodičom elektriny a majú nízku teplotu topenia a teplotu varu.
Porovnávacia tabuľka
| Iónové zlúčeniny | Molekulárne zlúčeniny | |
| Tvorenie | Iónové zlúčeniny sa tvoria v dôsledku elektrostatickej sily príťažlivosti medzi kovmi a nekovmi. | Molekulárne zlúčeniny sa tvoria v dôsledku zdieľania elektrónov medzi dvoma nekovmi. |
| skupina | Iónové zlúčeniny sa tvoria medzi kovmi a inými látkami. | Molekulárne zlúčeniny sa tvoria, keď sa dva nekovy chemicky kombinujú |
| dlhopis | Iónová zlúčenina sa vytvára v dôsledku elektrostatickej príťažlivej sily známej ako iónová väzba. | Molekulárne zlúčeniny sa tvoria vďaka kovalentnej väzbe medzi prvkami. |
| Teplota topenia a teplota varu | vysoký | nízky |
| Štát | Iónové zlúčeniny sú vždy v pevnom stave a tvoria kryštalický vzhľad. | Molekulové zlúčeniny môžu byť v akomkoľvek stave, pevné, kvapalné alebo plynné pri teplote miestnosti. |
| Dirigent elektriny | dobrý | zlý |
Čo sú to iónové zlúčeniny?
Tieto zlúčeniny sa tvoria v dôsledku elektrostatickej sily príťažlivosti medzi kovmi a nekovmi. Zjednodušene povedané, sila (iónová väzba) v tomto spôsobí, že pozitívne a negatívne nabité reagujú spolu za vzniku zlúčeniny. Obvykle sa iónové zlúčeniny objavujú v predávanom kryštalickom stave a sú dobrými vodičmi elektriny s vysokou teplotou topenia a teplotou varu. Iónové zlúčeniny sa tvoria medzi kovmi a nekovmi a majú nejaký lesklý vzhľad.
Príklad: Stolová soľ (NaCl) je najbežnejším príkladom iónovej zlúčeniny. V tejto zostave je sodík (NA) kov, zatiaľ čo chlór (Cl) nie je kov, oba sú držané pohromade vďaka elektrostatickej silovej príťažlivosti medzi oboma.
Čo sú to molekulárne zlúčeniny?
Zlúčeniny tvorené zdieľaním elektrónov medzi nekovmi sú známe ako molekulárna zlúčenina. Prvky, ktoré tu reagujú, sú držané pohromade kvôli kovalentnej väzbe, a preto sa tieto zlúčeniny často označujú ako kovalentné zlúčeniny.Vo vzťahu k iónovej zlúčenine sú zlým vodičom elektriny a majú nízku teplotu topenia a teplotu varu.
Príklad: V ozóne (O3) sa kyslík kombinuje so zdieľaním elektrónov za vzniku ozónu.
Iónové zlúčeniny verzus molekulárne zlúčeniny
- Iónové zlúčeniny sa tvoria v dôsledku elektrostatickej sily príťažlivosti medzi kovmi a nekovmi, zatiaľ čo molekulárne zlúčeniny sa tvoria v dôsledku zdieľania elektrónov medzi dvoma nekovmi.
- Molekulárne zlúčeniny sa tvoria, keď sa dve nekovové zlúčeniny chemicky kombinujú, na druhej strane sa tvoria iónové zlúčeniny medzi kovmi a inými látkami.
- Molekulárne zlúčeniny sa tvoria v dôsledku kovalentnej väzby medzi prvkami, zatiaľ čo iónová zlúčenina sa vytvára v dôsledku elektrostatickej sily príťažlivosti známej ako iónová väzba.
- Molekulové zlúčeniny majú v porovnaní s iónovými zlúčeninami nízku teplotu topenia a teplotu varu.
- Molekulárne zlúčeniny môžu byť v akomkoľvek stave, tuhé, kvapalné alebo plynné pri teplote miestnosti, zatiaľ čo iónové zlúčeniny sú vždy v pevnom stave a tvoria kryštalický vzhľad.
- Molekulárne zlúčeniny sú zlým vodičom elektriny, zatiaľ čo iónové zlúčeniny sú dobrým vodičom elektriny.