Obsah
- Hlavný rozdiel
- Ekvivalenčný bod vs. koncový bod
- Porovnávacia tabuľka
- Čo je bod ekvivalencie?
- Metódy stanovenia bodu ekvivalencie
- Čo je Endpoint?
- Kľúčové rozdiely
- záver
Hlavný rozdiel
Hlavným rozdielom medzi bodom ekvivalencie a koncovým bodom je ten bod ekvivalencie, ktorým je presný konečný bod, v ktorom chemická reakcia zvyčajne končí, zatiaľ čo koncový bod je limit, v ktorom dochádza k zmene farby v usporiadaní.
Ekvivalenčný bod vs. koncový bod
Bod ekvivalencie je presný bod, kde chemická reakcia končí v titračnej zmesi, zatiaľ čo koncový bod je bod, v ktorom dochádza k zmene farby v usporiadaní. Bod ekvivalencie poskytuje ten bod, v ktorom neznámy analyt úplne reagoval s titrantom a reakciami, končí, zatiaľ čo koncový bod nie vždy poskytuje ten bod, v ktorom neznáma analytika úplne reagovala s titrantom. V bode ekvivalencie zmena farby v reakčnej zmesi nešpecifikuje vždy konkrétny bod ekvivalencie; na druhej strane v koncovom bode zmena farby vždy označuje koncový bod. Bod ekvivalencie prichádza pred koncový bod; naopak, koncový bod je za bodom rovnocennosti. Slabé kyseliny v bode ekvivalencie môžu mať bod viacnásobnej ekvivalencie; naopak, slabé kyseliny v koncovom bode môžu mať iba jeden koncový bod. Bod ekvivalencie nastane, keď sa štandardný roztok, počet mólov titrantu, rovná počtu mólov analytu a roztoku s neznámymi koncentráciami; na druhej strane, koncový bod nastane, keď dôjde k zmene farby v reakcii. Ďalším bodom ekvivalencie je to, že titrant úplne reagoval s analytom, zatiaľ čo keď existujú signály dokončenia titrácie, je to koncový bod reakčnej zmesi. Ak pH titrantu zodpovedá pH v bode ekvivalencie, potom sa môže súčasne vyskytnúť bod ekvivalencie a koncový bod.
Porovnávacia tabuľka
| Bod ekvivalencie | Endpoint |
| Bod ekvivalencie je presný limit, keď sa chemická reakcia zastaví v titračnej kombinácii. | Koncový bod je bod, v ktorom dochádza k zmene farby v usporiadaní. |
| stechiometrie | |
| Poskytuje bod, v ktorom neznámy analyt úplne reagoval s titrantom a reakcia skončila | Nie vždy sa uvádza bod, v ktorom neznámy analytik úplne reagoval s titrantom |
| Zmena farby | |
| Nie vždy špecifikuje konkrétny bod rovnocennosti | Vždy označuje koncový bod |
| Koniec reakcie | |
| Predchádza koncovému bodu | Prichádza za bod ekvivalencie |
| Slabé kyseliny | |
| Môže mať viacnásobný ekvivalentný bod | Môže mať iba jeden koncový bod |
| Miesto výskytu | |
| Vyskytne sa, keď sa štandardný roztok, počet mólov titrantu, rovná počtu mólov analytu a roztoku s neznámymi koncentráciami | Vyskytuje sa pri zmene farby v reakcii |
| Ďalší priemer definícií | |
| Bod ekvivalencie je ten, že titrant úplne reagoval s analytom | Ak existujú signály dokončenia titrácie, je to koncový bod reakčnej zmesi |
Čo je bod ekvivalencie?
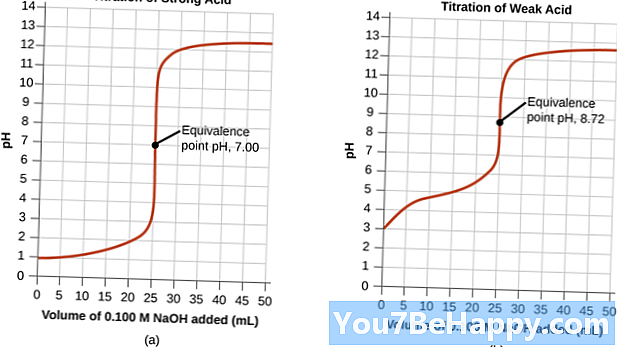
Bod ekvivalencie je presný bod, v ktorom chemická reakcia končí v titračnej zmesi. Ďalším bodom ekvivalencie je to, že titrant úplne reagoval s analytom. Bod ekvivalencie poskytuje tento hlavný limit, keď neidentifikovaný analyt úplne reagoval s reakciami a titroval. V bode ekvivalencie zmena farby reakčnej kombinácie všeobecne nešpecifikuje konkrétne bod ekvivalencie. Bod ekvivalencie nastane, keď sa štandardný roztok, počet mólov titrantu, rovná počtu mólov analytu a roztoku s neznámymi koncentráciami. Ekvivalenčný bod sa zvyčajne vždy dostane pred dosah koncového bodu.
Metódy stanovenia bodu ekvivalencie
- Zmena farby ukazovateľov: Prítomnosť farebnej transformácie určuje bod ekvivalencie pomocou autoindikátorov ako reaktantov v reakciách, pretože sa nepoužívajú skutočné indikátory.
- spektroskopia: Môže byť užitočný pri poskytovaní farebných reakčných zmesí.
- vodivosť: Môže byť tiež užitočné riadiť bod ekvivalencie titrácie.
- koncových bodov: Bod ekvivalencie sa niekedy môže považovať za koncový bod, pretože je takmer rovnaký.
Čo je Endpoint?
Koncový bod je bod, v ktorom dochádza k zmene farby v usporiadaní. Ďalším prostriedkom koncového bodu je to, že keď existujú signály dokončenia titrácie, je to koncový bod reakčnej zmesi. Koncový bod zvyčajne neponúka neustále tento obmedzený bod, keď neidentifikovaná analytička úplne reagovala s titrantom. V koncovom bode zmena farby obvykle vždy určuje koncový bod. Koncový bod sa obvykle vždy odvodzuje vedľa bodu ekvivalencie. Slabé kyseliny v koncovom bode môžu mať iba jeden koncový bod. Koncový bod nastane, keď dôjde k zmene farby v reakcii. V rôznych reakciách sledovaného parametra, keď sa zavedú samodiagnostické ukazovatele, keď celé množstvo neidentifikovaného reaktantu úplne reaguje s titrantom, sa potom stanoví limit.
Kľúčové rozdiely
- Bod ekvivalencie je presný limit, keď chemická reakcia končí v titračnej kombinácii, zatiaľ čo koncový bod je limit, v ktorom dochádza k zmene farby v postupe.
- Bod ekvivalencie poskytuje ten bod, v ktorom neznámy analyt úplne reagoval s titrantom a reakciami, končí, zatiaľ čo koncový bod nie vždy poskytuje ten bod, v ktorom neznáma analytika úplne reagovala s titrantom.
- V bode ekvivalencie zmena farby v reakčnej zmesi nešpecifikuje vždy konkrétny bod ekvivalencie; na druhej strane v koncovom bode zmena farby vždy označuje koncový bod.
- Bod ekvivalencie prichádza pred koncový bod; naopak, koncový bod je za bodom rovnocennosti.
- Slabé kyseliny v bode ekvivalencie môžu mať bod viacnásobnej ekvivalencie; naopak, slabé kyseliny v koncovom bode môžu mať iba jeden koncový bod.
- Bod ekvivalencie nastane, keď sa štandardný roztok, počet mólov titrantu, rovná počtu mólov analytu a roztoku s neznámymi koncentráciami; na druhej strane, koncový bod nastane, keď dôjde k zmene farby v reakcii.
- Ďalším bodom ekvivalencie je to, že titrant úplne reagoval s analytom, zatiaľ čo keď existujú signály dokončenia titrácie, je to koncový bod reakčnej zmesi.
- Ak pH titrantu zodpovedá pH v bode ekvivalencie, potom sa môže súčasne vyskytnúť bod ekvivalencie a koncový bod.
záver
Uvedená diskusia dospela k záveru, že bod ekvivalencie je presný koncový bod, v ktorom končí chemická reakcia a zmena farby v reakčnej zmesi nešpecifikuje vždy konkrétny bod ekvivalencie, zatiaľ čo koncový bod je limit, v ktorom k zmene farby dochádza v usporiadaní.